Шаблон:События дня:02-18
Admin (обсуждение | вклад) (Новая страница: «left 18 февраля 1913 — Фредерик Содди предлагает термин «изотоп». Изото…») |
Admin (обсуждение | вклад) |
||
| Строка 3: | Строка 3: | ||
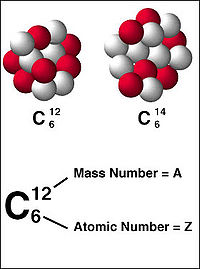
18 февраля 1913 — Фредерик Содди предлагает термин «изотоп». | 18 февраля 1913 — Фредерик Содди предлагает термин «изотоп». | ||
| − | Изотопы (от др. греч. ισος — «одинаковый», «равный», и τόπος — «место») — это разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковый атомный номер, но при этом разные массовые числа. Такое название связано с тем фактом, что все изотопы одного атома помещаются в одно и то же место (в одну клетку) таблицы Менделеева. Химические свойства атома зависят от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z, и практически не зависят от его массового числа A. Все изотопы одного элемента имеют одинаковый заряд ядра, при этом в них отличается только количество нейтронов. Как правило изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, который обозначает массовое число. | + | Изотопы (от др. греч. ισος — «одинаковый», «равный», и τόπος — «место») — это разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковый атомный номер, но при этом разные массовые числа. Такое название связано с тем фактом, что все изотопы одного атома помещаются в одно и то же место (в одну клетку) таблицы Менделеева. Химические свойства атома зависят от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z, и практически не зависят от его массового числа A. Все изотопы одного элемента имеют одинаковый заряд ядра, при этом в них отличается только количество нейтронов. Как правило изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, который обозначает массовое число. ''([[18_Февраля|далее…]])'' |
Текущая версия на 15:26, 18 февраля 2013
18 февраля 1913 — Фредерик Содди предлагает термин «изотоп».
Изотопы (от др. греч. ισος — «одинаковый», «равный», и τόπος — «место») — это разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковый атомный номер, но при этом разные массовые числа. Такое название связано с тем фактом, что все изотопы одного атома помещаются в одно и то же место (в одну клетку) таблицы Менделеева. Химические свойства атома зависят от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z, и практически не зависят от его массового числа A. Все изотопы одного элемента имеют одинаковый заряд ядра, при этом в них отличается только количество нейтронов. Как правило изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, который обозначает массовое число. (далее…)